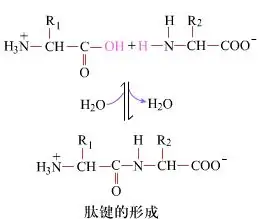
გარეგნულად, პეპტიდური ობლიგაციების ფორმირება, დიპეპტიდების წარმოქმნით, მარტივი ქიმიური პროცესია.ეს ნიშნავს, რომ ამინომჟავის ორი კომპონენტი უკავშირდება პეპტიდურ კავშირს, ამიდურ კავშირს, დეჰიდრატაციის დროს.
პეპტიდური ბმის ფორმირება არის ამინომჟავის გააქტიურება რბილი რეაქციის პირობებში.(A) კარბოქსილის ნაწილი, მეორე ამინომჟავა (B) ნუკლეოფილური გააქტიურებული კარბოქსილის ნაწილი ქმნის დიპეპტიდს (AB).თუ კარბოქსილის კომპონენტი (A) არ არის დაცული, პეპტიდური ბმის წარმოქმნა ვერ კონტროლდება.ქვეპროდუქტები, როგორიცაა ხაზოვანი და ციკლური პეპტიდები, შეიძლება შერეული იყოს სამიზნე ნაერთებთან AB.ამიტომ, ყველა ფუნქციური ჯგუფი, რომელიც არ არის ჩართული პეპტიდური ბმის ფორმირებაში, დაცული უნდა იყოს დროებით შექცევადად პეპტიდის სინთეზის დროს.
ასე რომ, პეპტიდების სინთეზი - თითოეული პეპტიდური ბმის ფორმირება - მოიცავს აგრეგაციის სამ საფეხურს.
პირველი ნაბიჯი არის ამინომჟავების მომზადება, რომლებსაც დაცვა სჭირდებათ და ამინომჟავების ცვიტერიონული სტრუქტურა აღარ არსებობს.
მეორე საფეხური არის ორსაფეხურიანი რეაქცია პეპტიდური ბმების ფორმირებისთვის, რომელშიც N-დაცული ამინომჟავის კარბოქსილის ჯგუფი ჯერ აქტიურდება აქტიურ შუალედში და შემდეგ წარმოიქმნება პეპტიდური ბმა.ეს დაწყვილებული რეაქცია შეიძლება მოხდეს როგორც ერთსაფეხურიანი ან ორი თანმიმდევრული რეაქციის სახით.
მესამე ნაბიჯი არის დამცავი ბაზის შერჩევითი მოცილება ან სრული მოხსნა.მიუხედავად იმისა, რომ ყველა მოცილება შეიძლება მოხდეს მხოლოდ მას შემდეგ, რაც ყველა პეპტიდური ჯაჭვი შეიკრიბება, ასევე საჭიროა დამცავი ჯგუფების შერჩევითი მოცილება პეპტიდის სინთეზის გასაგრძელებლად.
იმის გამო, რომ 10 ამინომჟავა (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec და Cys) შეიცავს გვერდითი ჯაჭვის ფუნქციურ ჯგუფებს, რომლებიც საჭიროებენ შერჩევით დაცვას, რაც ართულებს პეპტიდების სინთეზს.დროებითი და ნახევრად მუდმივი დაცვის ბაზები უნდა განვასხვავოთ სელექციურობის განსხვავებული მოთხოვნების გამო.დროებითი დაცვის ჯგუფები გამოიყენება შემდეგ ეტაპზე ამინომჟავების ან კარბოქსილის ფუნქციური ჯგუფების დროებითი დაცვის ასახვისთვის.ნახევრად მუდმივი დამცავი ჯგუფები ამოღებულია უკვე წარმოქმნილი პეპტიდური ბმების ან ამინომჟავების გვერდითი ჯაჭვების ჩარევის გარეშე, ზოგჯერ სინთეზის დროს.
იდეალურ შემთხვევაში, კარბოქსილის კომპონენტის გააქტიურება და პეპტიდური ბმების შემდგომი ფორმირება (დაწყვილების რეაქციები) უნდა იყოს სწრაფი, რაცემიის ან ქვეპროდუქტის წარმოქმნის გარეშე და მაღალი მოსავლიანობის მისაღწევად უნდა იქნას გამოყენებული მოლარული რეაქტორები.სამწუხაროდ, არცერთი ქიმიური შეერთების მეთოდი არ აკმაყოფილებს ამ მოთხოვნებს და რამდენიმე მათგანი შესაფერისია პრაქტიკული სინთეზისთვის.
პეპტიდების სინთეზის დროს, სხვადასხვა რეაქციებში ჩართული ფუნქციური ჯგუფები, როგორც წესი, დაკავშირებულია მანუალურ ცენტრთან, გლიცინი ერთადერთი გამონაკლისია და არსებობს როტაციის პოტენციური რისკი.
პეპტიდების სინთეზის ციკლის ბოლო ნაბიჯი არის ყველა დამცავი ჯგუფის მოცილება.დამცავი ჯგუფების შერჩევითი მოცილება მნიშვნელოვანია პეპტიდური ჯაჭვის გაფართოებისთვის, დიპეპტიდის სინთეზში დაცვის სრული მოხსნის მოთხოვნის გარდა.სინთეტიკური სტრატეგიები ყურადღებით უნდა იყოს დაგეგმილი.სტრატეგიული არჩევანიდან გამომდინარე, N-ს შეუძლია შერჩევითად ამოიღოს α-ამინო ან კარბოქსილის დამცავი ჯგუფები.ტერმინი "სტრატეგია" ეხება ცალკეული ამინომჟავების კონდენსაციის რეაქციების თანმიმდევრობას.ზოგადად, განსხვავებაა თანდათანობით სინთეზსა და ფრაგმენტების კონდენსაციას შორის.პეპტიდების სინთეზი (ასევე ცნობილია როგორც "ჩვეულებრივი სინთეზი") ხდება ხსნარში.უმეტეს შემთხვევაში, პეპტიდური ჯაჭვის თანდათანობითი გახანგრძლივება შესაძლებელია მხოლოდ პეპტიდური ჯაჭვის გამოყენებით უფრო მოკლე ფრაგმენტების სინთეზირებისთვის.უფრო გრძელი პეპტიდების სინთეზისთვის, სამიზნე მოლეკულები უნდა დაიყოს შესაბამის ფრაგმენტებად და დადგინდეს, რომ მათ შეუძლიათ მინიმუმამდე დაიყვანონ დიფერენციაციის ხარისხი C ბოლოში.ცალკეული ფრაგმენტების თანდათანობით აწყობის შემდეგ, სამიზნე ნაერთი შეუერთდება.პეპტიდის სინთეზის სტრატეგია მოიცავს საუკეთესო და შესაფერისი დამცავი ფრაგმენტის შერჩევას, ხოლო პეპტიდის სინთეზის სტრატეგია მოიცავს დამცავი ბაზების ყველაზე შესაფერისი კომბინაციისა და ფრაგმენტების კონიუგაციის საუკეთესო მეთოდს.
გამოქვეყნების დრო: ივლის-19-2023